4.3. Уравнения энергетического баланса для реактора в целом.
Выше определена величина потока воздуха в Ш.Р.,
обеспечивающая получение требуемого
соотношения (Н2 + СО) : N2 на выходе Ш.Р.
при заданной степени превращения метана ![]() 4.
Для нахождения условий, при которых степень
превращения метана будет достаточно высокой,
необходимо составить энергетический баланс для
реактора в целом.
4.
Для нахождения условий, при которых степень
превращения метана будет достаточно высокой,
необходимо составить энергетический баланс для
реактора в целом.
Интегральное уравнение баланса энергии для Ш.Р. характеризует совокупность происходящих в реакторе трансформаций энергии: превращение химической энергии окисляемых веществ в тепловую в головной части реактора и последующее обратное превращение в катализаторном слое тепловой энергии смеси реагентов в химическую энергию продуктов эндотермической реакции конверсии. Интегральное уравнение не должно включать температуру Т* адиабатного разогрева, являющуюся внутренним параметром процесса.
Воспользуемся уравнениями (19) для расчета абсолютной величины каждого из слагаемых в уравнении баланса энергии для адиабатного процесса (40). Как и в предшествующем разделе, температуру воздуха на входе 3 в Ш.Р. считаем равной температуре Т2 смешиваемых с ним газов, выходящих из реакционных труб Т.П. (рис.4). С учетом того, что потоки азота и аргона не изменяются от входа к выходу Ш.Р., имеем:
0 = ![]() HH2(T4)+
HH2(T4)+![]() HCH4(T4)+
HCH4(T4)+![]() HCO(T4)+
HCO(T4)+![]() HH2O(T4)+
HH2O(T4)+![]() HCO2(T4)+
HCO2(T4)+![]() HN2(Т4)+
HN2(Т4)+![]() HAr (Т4)–
HAr (Т4)–![]() HH2(T2)–
HH2(T2)–![]() HCH4(T2)–
HCH4(T2)–![]() HCO(T2)–
HCO(T2)–![]() HH2O(T2)–
HH2O(T2)–![]() HCO2(T2)–
HCO2(T2)–![]() HN2 (Т2)–
HN2 (Т2)–![]() HAr (Т2)–
HAr (Т2)–![]() HO2(T2) .
(45)
HO2(T2) .
(45)
Подставим в (45) значения рассчитанных ранее потоков веществ на входах и выходах Ш.Р. (9) – (12) и (34) – (37):
0 = [![]() (3
(3![]() 4+
4+![]() 4)–2
4)–2![]() ]HH2(T4)+
]HH2(T4)+![]() (1–
(1–![]() 4)HCH4 (T4)+
4)HCH4 (T4)+![]() (
(![]() 4–
4–![]() 4)HCO(T4)+[
4)HCO(T4)+[![]()
(![]() –
– ![]() 4–
4–![]() 4)+2
4)+2![]() ]HH2O(T4)+
]HH2O(T4)+![]() c 4HCO2(T4)+
c 4HCO2(T4)+![]() HN2(T4)+
HN2(T4)+![]() HAr(T4)–
HAr(T4)–![]() (3
(3![]() 2+
2+![]() 2)HH2(T2)–
2)HH2(T2)–![]() (1–
(1–![]() 2)HCH4(T2)–
2)HCH4(T2)–![]() (
(![]() 2–
2– ![]() 2 )HCO(T2)–
2 )HCO(T2)–![]() (
(![]() –
– ![]() 2–
2– ![]() 2 )HH2O
(T2)–
2 )HH2O
(T2)–![]()
![]() 2 HCO2(T2)–
2 HCO2(T2)–![]() HN2 (T2)–
HN2 (T2)–![]() HAr (T2)–
HAr (T2)–![]() HO2 (T2) =
HO2 (T2) =
![]() [
[![]() 4(3HH2(T4)+HCO(T4)
– HCH4(T4) – HH2O(T4))
–
4(3HH2(T4)+HCO(T4)
– HCH4(T4) – HH2O(T4))
–
–![]() 2(3HH2(T2)+HCO(T2)
– HCH4(T2) – HH2O(T2))]+
2(3HH2(T2)+HCO(T2)
– HCH4(T2) – HH2O(T2))]+![]() [2HH2O(T4)–2HH2(T4)–HO2(T2)]+
[2HH2O(T4)–2HH2(T4)–HO2(T2)]+![]()
![]() 4[HH2(T4)+
4[HH2(T4)+
+HCO2(T4)–HCO(T4)–HH2O(T4)]
– ![]()
![]() 2[HH2(T2)+HCO2(T2)–HCO(T2)
– HH2O(T2)]+
2[HH2(T2)+HCO2(T2)–HCO(T2)
– HH2O(T2)]+![]() [HCH4
(T4) – HCH4 (T2)]+
[HCH4
(T4) – HCH4 (T2)]+![]()
![]() [HH2O
(T4) – HH2O (T2)]+
[HH2O
(T4) – HH2O (T2)]+![]() [HN2 (T4)
– HN2 (T2)]+
[HN2 (T4)
– HN2 (T2)]+![]() [HAr (T4) – HAr (T2)]
. (46)
[HAr (T4) – HAr (T2)]
. (46)
Сгруппировав энтальпии веществ таким образом, чтобы выделить тепловые эффекты реакций (1) – (3), получим:
0 = ![]() [HCH4(T4)
– HCH4 (T2)]+
[HCH4(T4)
– HCH4 (T2)]+![]()
![]() [HH2O (T4)
–HH2O (T2)]+
[HH2O (T4)
–HH2O (T2)]+ ![]() [HO2 (T4) – HO2(T2)]
+
[HO2 (T4) – HO2(T2)]
+![]() [HN2(T4)
– HN2 (T2)]+
[HN2(T4)
– HN2 (T2)]+![]() [HAr(T4) – HAr (T2)]+
[HAr(T4) – HAr (T2)]+
![]() [
[![]() 4
4![]() 1H(T4)
–
1H(T4)
– ![]() 2
2![]() 1H(T2)]+
1H(T2)]+![]() [
[ ![]() 4
4![]() 2H(T4)–
2H(T4)–
![]() 2
2![]() 2H(T2)]+
2H(T2)]+ ![]()
![]() 3H(T4)
. (47)
3H(T4)
. (47)
Уравнение баланса в форме (47) имеет следующую
ясную интерпретацию. Суммарная энтальпия
потоков на входе в Ш.Р. равна сумме энтальпий
исходных веществ (метана, воды и воздуха) плюс
изменение энтальпии, соответствующее протеканию
реакций (1) и (2) до степеней превращения ![]() 2 и
2 и ![]() 2,
причем все значения энтальпий берутся для
температуры T2. Энтальпия выходящего
потока равна сумме энтальпий тех же исходных
веществ плюс изменение энтальпии,
соответствующее протеканию реакций (1) и (2) до
степеней превращения
2,
причем все значения энтальпий берутся для
температуры T2. Энтальпия выходящего
потока равна сумме энтальпий тех же исходных
веществ плюс изменение энтальпии,
соответствующее протеканию реакций (1) и (2) до
степеней превращения ![]() 4 и
4 и ![]() 4 и полному протеканию
реакции (3); все значения энтальпий берутся для
температуры на выходе T4 . Разность
энтальпий потока на выходе и входящих потоков в
адиабатном процессе равна нулю.
4 и полному протеканию
реакции (3); все значения энтальпий берутся для
температуры на выходе T4 . Разность
энтальпий потока на выходе и входящих потоков в
адиабатном процессе равна нулю.
Кроме того, уравнение (47) показывает, что совокупность процессов, протекающих в Ш.Р., полностью характеризуется параметрами трех линейно независимых химических реакций (1) – (3). Уравнение баланса энергии можно записать и в любой другой форме, соответствующей произвольной линейной комбинации уравнений (1) – (3). Между прочим, это означает, что для записи интегрального уравнения баланса энергии в Ш.Р. не имеет значения, какой из маршрутов окисления горючих газов в головной части реактора в действительности преобладает (для расчета Т* это имеет значение).
Упражнение.
Покажите (путем составления линейных комбинаций из уравнений), что в системе (1) – (3) можно заменить уравнение (3) уравнением реакции окисления СО, либо реакции окисления СН4
Как было показано выше, для обеспечения нужного
состава конвертированной смеси на выходе Ш.Р.
поток кислорода в составе воздушного потока на
входе в Ш.Р. должен удовлетворять соотношению (38),
где ![]()
![]() 0.300 . Тогда,
согласно соотношениям (28),
0.300 . Тогда,
согласно соотношениям (28),
![]() =
=![]()
![]()
![]() 4
4 ![]() ;
; ![]() =
= 
![]()
![]() 4
4 ![]() .
.
Подставляя эти выражения потоков в (47), в
приближении постоянных теплоемкостей, т.е.
используя соотношения (26), после группировки всех
членов, содержащих ![]() 4 в качестве сомножителя, и
сокращения на величину
4 в качестве сомножителя, и
сокращения на величину ![]() ,
найдем:
,
найдем:
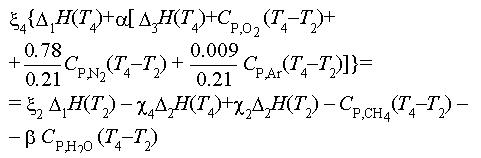 (48)
(48)
Величину ![]() 4 , входящую в уравнение (48),
можно оценить исходя из предположения о
квазиравновесности реакции (2), подобно тому, как
это делалось для реакционных труб Т.П.
4 , входящую в уравнение (48),
можно оценить исходя из предположения о
квазиравновесности реакции (2), подобно тому, как
это делалось для реакционных труб Т.П.
Константа равновесия для реакции (2) при температуре Т4 выражается как
КР,2(Т4 ) =  =
=  , (49)
, (49)
где ![]() и
и ![]() – парциальное давление и мольная
доля i-го газа на выходе Ш.Р.; мольная доля i-го
вещества в потоке 4 рассчитывается по уравнению
– парциальное давление и мольная
доля i-го газа на выходе Ш.Р.; мольная доля i-го
вещества в потоке 4 рассчитывается по уравнению ![]() =
=  (
(![]() – число веществ
в потоке 4).
– число веществ
в потоке 4).
Подставляя выражения потоков (35) – (37) с учетом (38) в (49), получим:
![]() [(3–2
[(3–2![]() )
) ![]() 4+
4+ ![]() 4]
4] ![]() 4–КР,2
4–КР,2![]() (
( ![]() 4 –
4 – ![]() 4 )[
4 )[ ![]() +
+
+(2![]() –1)
–1) ![]() 4 –
4 – ![]() 4] = 0 ,
4] = 0 ,
или
![]()
![]() 42 +
42 + ![]()
![]() 4 +
4 + ![]() = 0 , (50)
= 0 , (50)
где ![]() = 1–КР,2;
= 1–КР,2; ![]() = (3–2
= (3–2![]() )
)![]() 4 + КР,2
(
4 + КР,2
(![]() +2
+2![]()
![]() 4);
4);
![]() = –КР,2
= –КР,2![]() 4 [
4 [![]() +(2
+(2![]() –1)
–1)![]() 4] .
4] .
Коэффициент ![]() > 0, так
как
> 0, так
как ![]()
![]() 0.300 ;
0.300 ; ![]() < 0 в связи с тем, что
< 0 в связи с тем, что ![]() >
>![]() 4 . Дальнейшие рассуждения,
аналогичные тем, которые были приведены при
анализе уравнения (15) для Т.П., позволяют сделать
вывод, что у (50) существует единственное решение,
имеющее физический смысл:
4 . Дальнейшие рассуждения,
аналогичные тем, которые были приведены при
анализе уравнения (15) для Т.П., позволяют сделать
вывод, что у (50) существует единственное решение,
имеющее физический смысл:
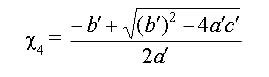 (51)
(51)
Таким образом, ![]() 4 является функцией
4 является функцией ![]() 4 и Т4
(через константу КР,2 ), аналогичной
функции
4 и Т4
(через константу КР,2 ), аналогичной
функции ![]() 2 от
2 от ![]() 2 и Т2 ,
определяемой уравнением (16).
2 и Т2 ,
определяемой уравнением (16).
Используя численные методы решения системы
уравнений, включающей уравнения (48), (16) и (51), а
также аппроксимационную зависимость КР,2 (Т)
(приведенную в таблице 1), можно рассчитать
функциональную зависимость между степенью
превращения метана и температурой на выходе Ш.Р. ![]() 4(Т4)
при заданных параметрах процесса первичного
реформинга
4(Т4)
при заданных параметрах процесса первичного
реформинга ![]() ,
, ![]() 2 и Т2
2 и Т2
Расчеты показывают, что в исследуемом
диапазоне параметров системы функция ![]() 4(Т4)
оказывается монотонно убывающей, т.е. повышение
степени конверсии должно сопровождаться
понижением температуры на выходе Ш.Р.
4(Т4)
оказывается монотонно убывающей, т.е. повышение
степени конверсии должно сопровождаться
понижением температуры на выходе Ш.Р.
Повышения степени конверсии в реакторе при
фиксированных ![]() ,
, ![]() 2 и Т2
можно добиться, например, за счет использования
более активного катализатора, либо увеличением
высоты катализаторного слоя при сохранении
величины нагрузки (расхода смеси) на единицу
площади поперечного сечения слоя.
Самосогласованное повышение степени конверсии
2 и Т2
можно добиться, например, за счет использования
более активного катализатора, либо увеличением
высоты катализаторного слоя при сохранении
величины нагрузки (расхода смеси) на единицу
площади поперечного сечения слоя.
Самосогласованное повышение степени конверсии ![]() 4 и
понижение температуры Т4 имеет свой
предел, определяемый химическим равновесием в
системе, который будет установлен в следующем
параграфе.
4 и
понижение температуры Т4 имеет свой
предел, определяемый химическим равновесием в
системе, который будет установлен в следующем
параграфе.
Приведем один из возможных алгоритмов расчета
функциональной зависимости между ![]() 4 и Т4 –
методом последовательных приближений. Данный
метод может быть реализован на простейшем
калькуляторе.
4 и Т4 –
методом последовательных приближений. Данный
метод может быть реализован на простейшем
калькуляторе.
Выражая тепловые эффекты реакций с помощью уравнения (23), преобразуем уравнение (48) к виду:
![]() 4 =
4 =  , (52)
, (52)
где ![]() =
= ![]() 2
2 ![]() 1H(298) + (
1H(298) + ( ![]() 2 –
2 – ![]() 4)
4) ![]() 2H(298);
2H(298);
a2 = ![]() 2
2 ![]() 1CP+
1CP+
![]() 2
2![]() 2CP; a3 = – (CP,CH4
+
2CP; a3 = – (CP,CH4
+ ![]() CP,H2O );
CP,H2O );
![]() = –
= – ![]() 4
4 ![]() 2CP ;
2CP ;
a5 = ![]() 1H(298) +
1H(298) + ![]()
![]() 3H(298) ;
3H(298) ;
a6 = ![]() (CP,O2 +
(CP,O2 + ![]() C P,N2 +
C P,N2 +
 C P,Ar ) ;
C P,Ar ) ;
a7 = ![]() 1CP
+
1CP
+ ![]()
![]() 3CP
.
3CP
.
Знаком "~" помечены те коэффициенты, которые изменяются при итерациях.
Заменив в (52) Т4 – Т2 на (Т4 – 298) – (Т2 – 298), окончательно получим:
![]() 4 =
4 =  , (53)
, (53)
В начальном приближении полагаем ![]() 4 =
4 = ![]() 2 и
рассчитываем
2 и
рассчитываем ![]() 4 по (53) для заданного
значения Т4 . Для полученного значения
4 по (53) для заданного
значения Т4 . Для полученного значения ![]() 4 определяем
4 определяем
![]() 4 по
формуле (51), пересчитываем коэффициенты
4 по
формуле (51), пересчитываем коэффициенты ![]() и
и ![]() и снова рассчитываем
и снова рассчитываем ![]() 4 по (53). Повторяя
процесс вычислений нужное число раз, можно
достичь требуемой точности расчета
4 по (53). Повторяя
процесс вычислений нужное число раз, можно
достичь требуемой точности расчета ![]() 4 . Для оценочных
расчетов достаточно ограничиться начальным
приближением, так как влияние поправок
относительно невелико. Величина
4 . Для оценочных
расчетов достаточно ограничиться начальным
приближением, так как влияние поправок
относительно невелико. Величина ![]() 2 при заданных
значениях
2 при заданных
значениях ![]() , р, Т2 и
, р, Т2 и ![]() 2 должна
быть рассчитана заранее.
2 должна
быть рассчитана заранее.