Ответ на задачу 3. (автор В.Н. Хвалюк)
Вещество А — (NH4)2Cr2O7
дихромат аммония (бихромат аммония). Процесс
"извержения вулкана" можно приблизительно
выразить уравнением:
(NH4)2Cr2O7 Cr2O3 + N2
+ 4H2O.
Для реакции A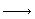 B уменьшение массы
навески (масса газообразных продуктов реакции)
составило 15,13 - 12,06 = 3,07 (г) или 20,29%. Газообразными
продуктами реакции разложения дихромата аммония
могут быть: аммиак, азот (в результате окисления
аммиака) и пары воды. Т.о. в колонке с NaOH
поглощаются пары воды (
B уменьшение массы
навески (масса газообразных продуктов реакции)
составило 15,13 - 12,06 = 3,07 (г) или 20,29%. Газообразными
продуктами реакции разложения дихромата аммония
могут быть: аммиак, азот (в результате окисления
аммиака) и пары воды. Т.о. в колонке с NaOH
поглощаются пары воды (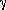 H2O = 2,16 : 18 = 0,12 моль).
Половина объема оставшихся газов поглощается
раствором серной кислоты, значит газы содержатся
в соотношении 1:1 (объемном и мольном). Масса
осушенного газа составляет 3,07 - 2,16 = 0,91 (г).
Количества аммиака и азота равны 0,91 : (28 + 17) = 0,02
(моль). Соотношение NH3:N2:H2O = 1:1:6
(моль), масса продуктов реакции с целочисленными
коэффициентами равна 17 + 28 + 108 = 153 (г), масса
исходного дихромата аммония составляет 153 : 0,2029 =
754 (г), количество — 754 : 252 = 2,99 (моль). Тогда
уравнение разложения на первой стадии может быть
записано:
H2O = 2,16 : 18 = 0,12 моль).
Половина объема оставшихся газов поглощается
раствором серной кислоты, значит газы содержатся
в соотношении 1:1 (объемном и мольном). Масса
осушенного газа составляет 3,07 - 2,16 = 0,91 (г).
Количества аммиака и азота равны 0,91 : (28 + 17) = 0,02
(моль). Соотношение NH3:N2:H2O = 1:1:6
(моль), масса продуктов реакции с целочисленными
коэффициентами равна 17 + 28 + 108 = 153 (г), масса
исходного дихромата аммония составляет 153 : 0,2029 =
754 (г), количество — 754 : 252 = 2,99 (моль). Тогда
уравнение разложения на первой стадии может быть
записано:
3 (NH4)2Cr2O7 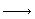 n B + N2
+ NH3 + 6 H2O,
n B + N2
+ NH3 + 6 H2O,
откуда, состав B - Cr2O5 NH3 (n=3);
3 (NH4)2Cr2O7 = 3 Cr2O5 NH3
+ N2 + NH3 + 6 H2O.
При превращении B 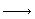 C уменьшение массы составляет
12,06 - 10,42 = 1,64 (г) или 13,60%. В составе газообразных
продуктов аммиак и азот (соотношение 1:1) и вода.
Т.к. в дальнейших превращениях не происходит
выделения ни азота ни аммиака, то на этой стадии
происходит полное удаление азотсодержащих
продуктов:
C уменьшение массы составляет
12,06 - 10,42 = 1,64 (г) или 13,60%. В составе газообразных
продуктов аммиак и азот (соотношение 1:1) и вода.
Т.к. в дальнейших превращениях не происходит
выделения ни азота ни аммиака, то на этой стадии
происходит полное удаление азотсодержащих
продуктов:
n Cr2O5*NH3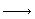 m C + NH3 +N2 +
k H2O,
m C + NH3 +N2 +
k H2O,
откуда n будет кратно 3 (1 + 2 — индексы при
азотсодержащих продуктах), тогда масса
газообразных продуктов равна 3(201 ?0,1360) = 82; масса
воды 82 - 17 -28 = 37; k = 37:18 = 2,06.
3 Cr2O5*NH3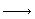 m C + N2 + NH3 + 2 H2O.
m C + N2 + NH3 + 2 H2O.
Отсюда состав m C — Cr6O13H2
или (CrO2)6? H2O, хотя нельзя
однозначно сказать входит ли вода в состав
продукта, или это гидроксо-группы.
3 Cr2O5 *NH3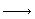 (CrO2)6 H2O
+ NH3 + N2 + 2 H2O.
(CrO2)6 H2O
+ NH3 + N2 + 2 H2O.
Содержание кислорода в (CrO2)6 * H2O
— 39,85%.
При дальнейшем нагревании происходит
уменьшение массы на 3,26%, что соответствует
удалению 522*0,0326 = 17 (г), т.е. полной дегидратации.
(CrO2)6* H2O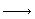 6 CrO2 + H2O
6 CrO2 + H2O
Содержание кислорода в CrO2 составляет 38,10%.
Дальнейшее нагревание приводит к разложению CrO2.
4 CrO2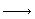 2Cr2O3 + O2.
2Cr2O3 + O2.
Суммируя все стадии разложения, получаем:
6 (NH4)2Cr2O7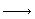 6 Cr2O3 + 4
N2 + 4 NH3 + 18 H2O + 3O2.
6 Cr2O3 + 4
N2 + 4 NH3 + 18 H2O + 3O2.
Эти данные были опубликованы в работе:
B.Mahieu, D.J.Apers, P.C.Capron "Thermal decomposition of ammonium
dichromate"
J. Inorg. Nucl. Chem., 1971, v.33, p.2857 - 2866.
![]() B уменьшение массы
навески (масса газообразных продуктов реакции)
составило 15,13 - 12,06 = 3,07 (г) или 20,29%. Газообразными
продуктами реакции разложения дихромата аммония
могут быть: аммиак, азот (в результате окисления
аммиака) и пары воды. Т.о. в колонке с NaOH
поглощаются пары воды (
B уменьшение массы
навески (масса газообразных продуктов реакции)
составило 15,13 - 12,06 = 3,07 (г) или 20,29%. Газообразными
продуктами реакции разложения дихромата аммония
могут быть: аммиак, азот (в результате окисления
аммиака) и пары воды. Т.о. в колонке с NaOH
поглощаются пары воды (![]() H2O = 2,16 : 18 = 0,12 моль).
Половина объема оставшихся газов поглощается
раствором серной кислоты, значит газы содержатся
в соотношении 1:1 (объемном и мольном). Масса
осушенного газа составляет 3,07 - 2,16 = 0,91 (г).
Количества аммиака и азота равны 0,91 : (28 + 17) = 0,02
(моль). Соотношение NH3:N2:H2O = 1:1:6
(моль), масса продуктов реакции с целочисленными
коэффициентами равна 17 + 28 + 108 = 153 (г), масса
исходного дихромата аммония составляет 153 : 0,2029 =
754 (г), количество — 754 : 252 = 2,99 (моль). Тогда
уравнение разложения на первой стадии может быть
записано:
H2O = 2,16 : 18 = 0,12 моль).
Половина объема оставшихся газов поглощается
раствором серной кислоты, значит газы содержатся
в соотношении 1:1 (объемном и мольном). Масса
осушенного газа составляет 3,07 - 2,16 = 0,91 (г).
Количества аммиака и азота равны 0,91 : (28 + 17) = 0,02
(моль). Соотношение NH3:N2:H2O = 1:1:6
(моль), масса продуктов реакции с целочисленными
коэффициентами равна 17 + 28 + 108 = 153 (г), масса
исходного дихромата аммония составляет 153 : 0,2029 =
754 (г), количество — 754 : 252 = 2,99 (моль). Тогда
уравнение разложения на первой стадии может быть
записано: