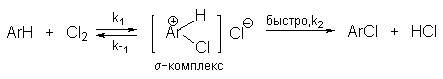
3.2. Галогенирование
В реакциях замещения аренового водорода на галогены активность галогенов уменьшается в ряду Cl2>Br2>>I2. В качестве электрофильных галогенирующих агентов используются молекулярные галогены или комплексы галогенов с разнообразными кислотами Льюиса (FeCl3, FeBr3, AlCl3, AlBr3 галогениды Ga,Sb,Sn,TiCl4 и др.). Очень часто применяют растворы Сl2 и Br2 в уксусной кислоте.
Галогенирование аренов молекулярными галогенами в отсутствие кислот Льюиса или Бренстеда, поляризующих связь галоген-галоген, эффективно лишь для полиалкилбензолов, фенолов, простых эфиров одно- и многоатомных фенолов, и ароматических аминов. В других случаях необходим катализ кислотами Льюиса или Бренстеда. Активные субстраты хлорируются хлором в уксусной кислоте, где электрофилом является просто элементарный хлор. Реакция имеет второй кинетический порядок (скорость=k[ArH][Cl2]). На ее скорость не влияют добавки сильных кислот или оснований. При добавлении ионов Cl- (общий ион) и СH3COO- в обоих случаях проявляется лишь нормальный солевой эффект. На основании этого можно сделать вывод, что электрофилами в этом случае не являются ни Cl+ , ни CH3COОCl. Поэтому был предложен очень простой двухстадийный механизм:
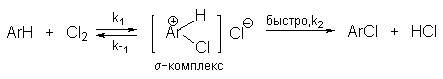
Такой же механизм наблюдается и в других органических растворителях.
Бромирование происходит аналогично, однако при сохранении первого порядка по ArH, порядок по брому часто отличается от первого. Вероятно, это связано с более легкой обратимостью первой стадии. Галогенирование свободными галогенами активных ароматических субстратов протекает очень легко и часто приводит к полигалоидпроизводным. Например, анилин и фенол при действии бромной воды мгновенно превращаются в нерастворимые 2,4,6-трибромпроизводные, причем в случае фенола при избытке бромной воды реакция протекает более глубоко.
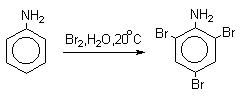
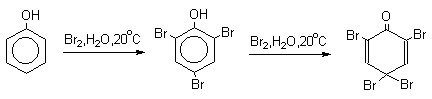
Поэтому, для получения моногалоидзамещенных производных фенола и анилина используют специальные приемы:
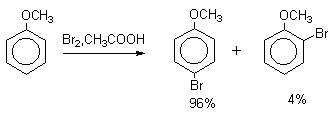
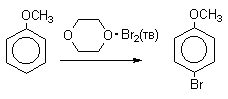
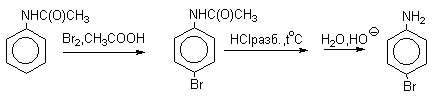
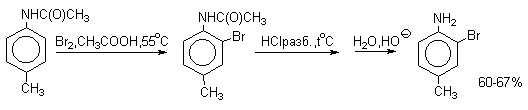
Механизм галогенирования при катализе
кислотами Льюиса или Бренстеда часто называют
галогенированием "положительным бромом"
или "положительным хлором", но эти названия
чисто условны. При бромировании бромом в
присутствии кислот Льюиса в этих реакциях
участвует комплекс галогена с кислотой Льюиса,
например, [Br![]() + ...Br-FeBr3
+ ...Br-FeBr3![]() - ]. В качестве катализатора
обычно берут FeCl3 или FeBr3, которые
можно получать из металлического железа и Cl2
или Br2 прямо в реакционном сосуде. Более
активные катализаторы AlCl3 или AlBr3
нередко приводят к образованию продуктов
полигалогенирования. Так, например, при
бромировании бензола в присутствии AlBr3
замещаются все шесть атомов водорода и
образуется гексабромбензол. Поэтому AlHal3
мало пригодны для галогенирования бензола, моно-
и диалкилбензолов, галогенбензолов. Сильные
кислоты Льюиса эффективны при галогенировании
нитробензола, бензойной кислоты и других
соединений, содержащих электроноакцепторные
заместители. Во всех случаях атакующим агентом,
по-видимому, является комплекс Hal2 с
кислотой Льюиса. До сих пор нет прямых
доказательств участия в реакции катионов Cl+
или Br+, как кинетически независимых частиц.
- ]. В качестве катализатора
обычно берут FeCl3 или FeBr3, которые
можно получать из металлического железа и Cl2
или Br2 прямо в реакционном сосуде. Более
активные катализаторы AlCl3 или AlBr3
нередко приводят к образованию продуктов
полигалогенирования. Так, например, при
бромировании бензола в присутствии AlBr3
замещаются все шесть атомов водорода и
образуется гексабромбензол. Поэтому AlHal3
мало пригодны для галогенирования бензола, моно-
и диалкилбензолов, галогенбензолов. Сильные
кислоты Льюиса эффективны при галогенировании
нитробензола, бензойной кислоты и других
соединений, содержащих электроноакцепторные
заместители. Во всех случаях атакующим агентом,
по-видимому, является комплекс Hal2 с
кислотой Льюиса. До сих пор нет прямых
доказательств участия в реакции катионов Cl+
или Br+, как кинетически независимых частиц.
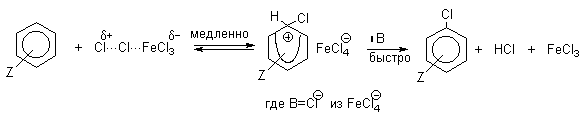
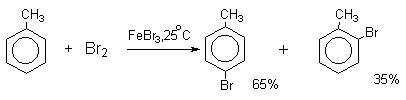
Толуол в присутствии FeBr3, бромируется существенно быстрее, чем бензол (kтолуол/kбензол=160). При этом получается смесь пара- и орто-изомеров в соотношении ~2:1, и совсем не получается мета-изомера, а при хлорировании толуола орто- и пара-изомеры образуются в примерно равных количествах.
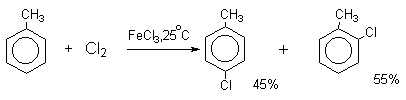
Следует также отметить, что введение хлора или брома в бензольное кольцо уменьшает скорость дальнейшего замещения не более чем в 7-8 раз в отличие от нитрования, где скорость реакции введения второго заместителя уменьшается в 107раз. Поэтому хлорирование и бромирование бензола всегда приводит к смеси дигалогенпроизводных. При хлорировании хлорбензола сначала образуется смесь орто- и пара-дихлорбензолов в соотношении 3:7, а при дальнейшем хлорировании получается смесь 1,2,3- и 1,2,4-трихлорбензолов.
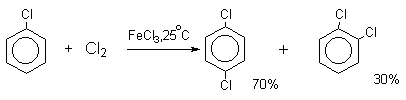
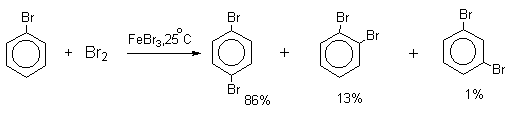
Напротив, каталитическое галогенирование соединений с электроноакцепторными заместителями протекает более селективно.
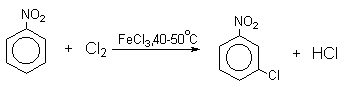
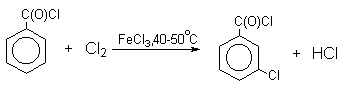
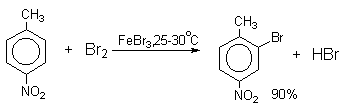
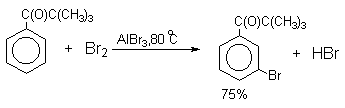
Нафталин галогенируется гораздо легче, чем бензол. Реакцию можно проводить как в присутствии кислоты Льюиса, так и без нее.
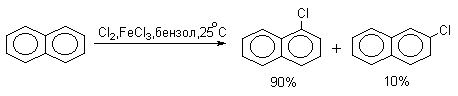
Бром реагирует еще более селективно, чем хлор:
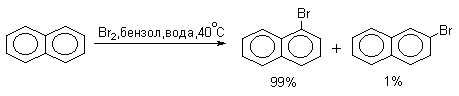
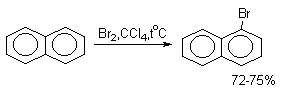
Широкое применение в синтетической практике находят такие галогенирующие агенты, как трифторацетилгипобромит и особенно трифторацетилгипоиодит (CF3COOHal). Эти гипогалогениты образуются при действии соответствующего галогена на трифторацетаты серебра или ртути.
![]()
![]()
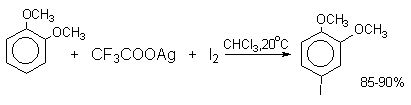
Можно использовать также ацетилгипогалогениты, однако трифторацетилгипогалогениты гораздо более реакционноспособны. Например, скорости бромирования при действии Br2, CH3COOBr и CF3COOBr составляют 1:106:1010.
Молекулярный иод является слишком слабым электрофильным агентом. Только очень активные ароматические соединения, такие, как ароматические амины или фенолят-ион реагируют непосредственно с I2. В качестве более активного иодирующего агента иногда используют хлорид иода ICl. Удобным методом иодирования ароматических соединений является использование смеси молекулярного иода и окислителей (окислительное иодирование), лучшим из которых является, по-видимому, HIO4, но азотная кислота употребляется наиболее часто, как более дешевая.
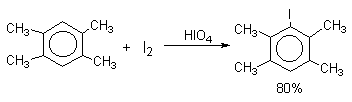
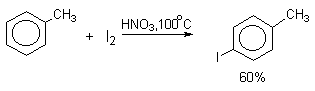
Очень хорошие результаты получаются при иодировании ароматических соединений смесью I2 с хлоридом меди (II) CuCl2. Хлорная медь выполняет, вероятно, двоякую функцию и кислоты Льюиса и окислителя:
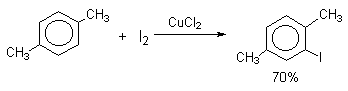
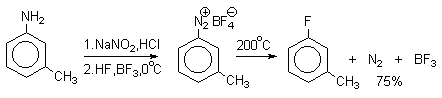
Ввиду чрезвычайной активности фтора, прямое фторирование практически не применяют для введения фтора в ароматическое кольцо. Арилфториды получают термическим разложением тетрафторборатов арилдиазониев (реакция Шимана).